La victoria de LivaNova en la FDA podría estar subestimando el margen de oportunidad para capturar el mercado que todavía no está explorado por los productos de OSA: entre el 20% y el 30%.
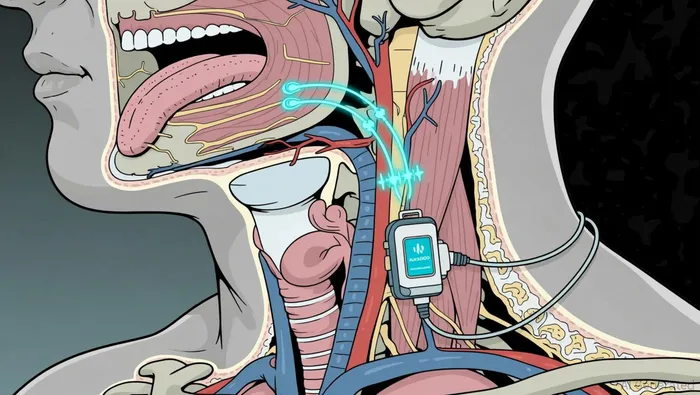
El catalizador inmediato es evidente. El 19 de marzo, la FDA otorgó la aprobación previa al mercado del sistema aura6000 de LivaNova. Esto marca el primer caso en que una terapia de estimulación del nervio hipogloso está aprobada en los Estados Unidos, sin tener contraindicaciones relacionadas con el colapso concéntrico del nervio. Este es un punto clave, ya que permite tratar a un grupo más amplio de pacientes, incluyendo aquellos con características anatómicas difíciles, un grupo que a menudo queda excluido por los competidores. La aprobación se basa en datos provenientes del estudio OSPREY, que demostró mejoras clínicamente significativas en el tratamiento de la apnea obstructiva del sueño.
La reacción inicial del mercado fue un aumento del 6% en las últimas cinco jornadas. Se trata de una respuesta positiva típica ante una importante victoria regulatoria. Sin embargo, las acciones siguen bajando un 9% en las últimas 20 jornadas. Esto indica que las noticias están siendo evaluadas en relación con otros factores importantes. La volatilidad es evidente; las acciones han variado casi un 4% durante el día. Esta reacción mixta prepara el terreno para una situación comercial complicada en el futuro.
El aurá6000 aprobado es el dispositivo de primera generación. Se espera que el sistema de próxima generación, compatible con la resonancia magnética, se lance en la primera mitad de 2027, en espera de una revisión adicional por parte de la FDA. Esto implica una implementación comercial en dos fases: primero se lanzará el dispositivo actual, y posteriormente, la versión más avanzada. La aprobación en sí es un paso importante, pero todavía faltan aproximadamente 18 meses para que se generen ingresos significativos gracias a este dispositivo.
La ventaja competitiva y las amenazas a corto plazo
La victoria de LivaNova en la FDA es un paso claro hacia adelante, pero su margen de oportunidades se está reduciendo rápidamente. La principal ventaja de la empresa es su capacidad para tratar a un grupo más amplio de pacientes. A diferencia del estándar actual de tratamiento proporcionado por Inspire, que excluye a los pacientes con colapso concéntrico completo, el ensayo Aura6000 de LivaNova incluyó deliberadamente a estos pacientes. Esto podría expandir el mercado elegible en un 20% a 30%. Además, el enfoque de la empresa elimina la necesidad de realizar una prueba de endoscopia para detectar el sueño inducido por medicamentos. Este procedimiento simplificado representa una ventaja operativa tangible.
Sin embargo, la amenaza competitiva a corto plazo es inmediata y sofisticada. Justo el mes pasado, la FDA aprobó el dispositivo Genio de Nyxoah. Se trata de una solución no implantable, sin plomo, y compatible con las resonancias magnéticas. Este dispositivo se adapta perfectamente a pacientes y médicos que buscan una opción menos invasiva, además de poder actualizar su tecnología sin necesidad de cirugías adicionales. El dispositivo de Nyxoah va dirigido directamente a la misma población de pacientes, lo que significa que el mercado se fragmentará antes incluso de que el sistema de próxima generación de LivaNova esté listo para su lanzamiento en el año 2027.
La presión competitiva se espera que aumente aún más. Se espera que se otorgue la aprobación para un dispositivo compatible con MRI a finales de 2026. Esto podría debilitar aún más la ventaja que LivaNova tiene como empresa que llega primero al mercado. Esto crea un entorno de lanzamiento muy competitivo, donde LivaNova enfrentará no solo Inspire, sino también otro nuevo competidor que no utiliza implantes, además de otra opción compatible con MRI. La ventaja clínica de la empresa, gracias al diseño riguroso de sus ensayos aleatorizados y al enfoque de estimulación nerviosa proximal, será crucial para ganar la preferencia de los médicos en este entorno tan complejo.
La evaluación y el análisis de riesgos/retribución
La aprobación de la FDA es un primer paso necesario, pero la verdadera cuestión es si el aumento del 6% en el precio de las acciones corresponde adecuadamente al valor que se espera en el largo plazo. El mercado de dispositivos para el tratamiento de la apnea del sueño es amplio y en constante crecimiento.8.52 mil millones de dólares en el año 2024Se proyecta que esta industria alcance los 12.92 mil millones de dólares estadounidenses para el año 2030. Sin embargo, el segmento específico de la neuroestimulación es mucho más pequeño.Casi 359 millones de dólares en el año 2023.Con un crecimiento anual promedio del 17%, esto representa el objetivo principal de LivaNova. Su principal diferenciador es la capacidad de captar una mayor parte de ese nicho de mercado.
La oportunidad depende de la posibilidad de comercializar sus ventajas clínicas. Al tratar a pacientes con colapso concéntrico completo, un grupo que se estima que constituye una parte importante de los pacientes que necesitan tratamiento.Del 20% al 30%La población de pacientes con OSA está excluida por la empresa Inspire. Esto permitiría a la empresa expandir significativamente su mercado objetivo. El proceso simplificado, que elimina la necesidad de realizar pruebas de sueño inducidas por medicamentos, es otra ventaja tangible. Pero existe el riesgo de que este beneficio se pierda antes de que pueda ser aprovechado en forma rentable. La FDA podría exigir posteriormente que LivaNova incluya una contraindicación para el uso del producto en pacientes con CCC. Esto socavaría sus argumentos clave. Esa incertidumbre regulatoria es un factor importante que debe tenerse en cuenta.
El riesgo de ejecución también es alto. La empresa debe lograr que su dispositivo de primera generación sea adoptado por los médicos, mientras que su sistema de próxima generación, compatible con las resonancias magnéticas, aún está en fase de desarrollo.Se espera que llegue a finales de 2026.Esto crea un entorno de lanzamiento muy competitivo. Solo el mes pasado, la FDA aprobó el dispositivo Genio de Nyxoah, una alternativa no implantable y sin plomo, que atrae a aquellos pacientes que buscan opciones menos invasivas. Se espera también que se apruebe otro dispositivo compatible con las imágenes por resonancia magnética a finales de 2026. LivaNova tendrá que competir con estos nuevos competidores por la atención de los pacientes y los médicos, incluso antes de que su propia plataforma avanzada esté lista.
En resumen, se trata de una apuesta de alto riesgo, en dos fases. El catalizador inmediato es la aprobación del proyecto, pero la valoración de las acciones debe reflejar el largo tiempo que falta para obtener ingresos significativos, así como la intensa competencia que existe en este sector. Un aumento del 6% es una reacción positiva, pero puede que eso no sea suficiente para superar los obstáculos y aprovechar al máximo la oportunidad para establecer una ventaja inicial en un sector que está a punto de volverse mucho más competitivo.

Comentarios
Aún no hay comentarios