Combinación de IDE397 + Trodelvy para cánceres de eliminación de MTAP: un avance en la oncología de precisión con un camino claro de la Fase 2
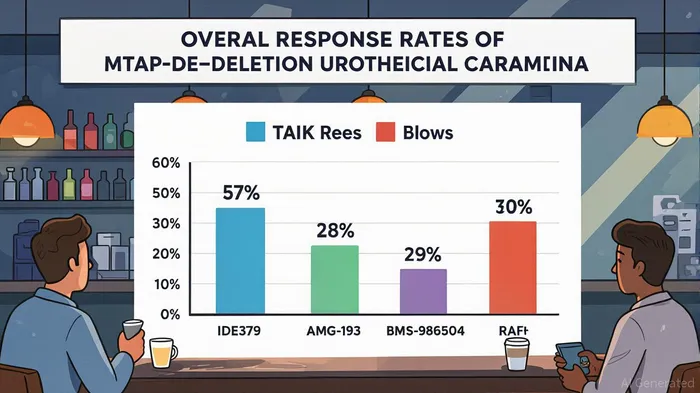
En el panorama en evolución de la oncología de precisión, la combinación de IDE397, un inhibidor de primera línea de metionina adenosiltransferasa 2 alfa (MAT2A), y Trodelvy (sacituzumab govitecan), un conjugado de anticuerpo y fármaco (ADC), ha surgido como un candidato convincente para cánceres con eliminación de MTAP. Los datos recientes de ensayos de fase 1/2 subrayan su validez clínica, con una tasa de respuesta general (ORR) del 57% observada en pacientes con cáncer urotelial con eliminación de MTAP en la dosis 2 (30 mg de IDE397 + 7,5 mg/kg de Trodelvy) y una tasa de control de la enfermedad del 100% en la misma cohorte]1]. Estos resultados, junto con un perfil de seguridad manejable, posición a esta combinación como un posible cambio de paradigma en el tratamiento de este subconjunto de tumores definido genómicamente.
Validez clínica: un enfoque sintético letal
Los cánceres por deleción de MTAP, que tienen lugar en el 10 al 15% de los tumores sólidos, incluido el cáncer de pulmón de células no pequeñas (NSCLC), el carcinoma urotelial y el cáncer de páncreas, constituyen una necesidad médica importante que no se ha cumplido. Estos tumores se caracterizan por la pérdida de laMTAPgen, lo que conduce a la acumulación de metiltioadenosina (MTA) y la subsiguiente vulnerabilidad a la inhibición del PRMT5.[2] No obstante, los inhibidores de PRMT5 existentes como AMG 193 (28 % de ORR) y BMS-986504 (29 % de ORR) afrontan problemas, incluyendo la resistencia de las células estromatarias que expresan MTAP en el microentorno tumoral[3]. IDE397, a la vez que se dirige a MAT2A, una enzima clave en la vía metabólica del MTA, completa la inhibición de PRMT5 mientras mejora la eficacia del ADC como Trodelvy. El ORR del 57% en la cohorte del nivel de dosificación 2 de IDE397 + Trodelvy supera las cifras históricas de la monoterapia y sugiere un mecanismo sinérgico[4].
La expansión del ensayo al NSCLC con pérdida de MTAP refuerza su importancia clínica, dado que este subconjunto representa el 15–20 % de los casos de NSCLC.[5] A partir de septiembre de 2025, se registrará el primer paciente de esta cohorte;IDEAYA BiocienciasIDYA--están listos para validar la versatilidad de la combinación; la selección de una dosis de la Fase 2 recomendada para finales de 2025 y actualizaciones anticipadas a principios de 2026 serán hitos críticos para los inversores[6]
Potencial comercial: apuntar a una oportunidad de $5 mil millones
El panorama comercial de las terapias de eliminación de la metil-transferasa se está madurando rápidamente. Con alrededor del 10-15% de todos los cánceres eliminados por la metil-transferasa, la población de pacientes es sustancial, en particular en indicaciones de alta prevalencia como son los cánceres uroteliales y de pulmón]7] Los analistas proyectan que los inhibidores del PRMT5 con éxito podrían alcanzar ventas máximas de $5000 millones en 2030, siempre que se aprueben las autorizaciones regulatorias para 2026.el8] El mecanismo dual de IDE397 + Trodelvy, que combina la orientación metabólica con la citotoxicidad mediada por el ADC, lo sitúa en una posición para captar una parte significativa de este mercado.
Trodelvy, ya aprobado para el cáncer urotelial, se beneficia de una designación de medicamento huérfano existente para indicaciones que eliminen el MTAP, lo que podría extender su exclusividad en el mercado.Son9]. Mientras tanto, la colaboración de IDE397 conGalaadGILD--garantiza el acceso a Trodelvy a escala, mitigando los riesgos de la cadena de suministro. Se estima que el mercado de ADC, en sí, crecerá a 50 mil millones de dólares para 2030, impulsado por innovaciones como la estrategia de combinación de IDE397[10]
Posicionamiento competitivo y mitigación de riesgos
Mientras que competidores comoTerapéutica del tangoTNGX--Están avanzando los inhibidores de PRMT5 (por ejemplo, TNG462 para cáncer de páncreas), el enfoque de doble acción de IDE397+Trodelvy ofrece una ventaja diferenciada. A diferencia de la monoterapia, la combinación aborda tanto el metabolismo de las células tumorales como la expresión del antígeno de superficie (Trop-2), lo que reduce las vías de resistencia. Además, la ausencia de eventos adversos graves relacionados con el tratamiento en los ensayos de dosis de fase 2 destaca su perfil favorable de riesgo-beneficio.[11].
Sin embargo, aún hay retos pendientes. La complejidad del microentorno tumoral, como el metabolismo del MTA por las células del estroma, podría afectar la efectividad en algunos pacientes[R]. La expansión planificada de IDEAYA en NSCLC y su desarrollo paralelo de IDE892, un inhibidor de PRMT5, tienen como objetivo solucionar estas brechas a través de estrategias de combinación.
Conclusiones: un avance en la oncología de precisión
La combinación de IDE397 + Trodelvy es un gran avance en la oncología de precisión gracias a su camino claro de Fase 2. Su eficacia clínica, el manejo de la seguridad y la alineación con el creciente mercado de ADC destaca su potencial para redefinir los estándares de tratamiento para los cánceres con deleción de MTAP. Para los inversores, la necesidad médica insatisfecha de la combinación, los sólidos datos de los ensayos y las asociaciones estratégicas con Gilead presentan un caso convincente para crear valor a largo plazo.IDEAYAIDYA--Avances hacia la Fase 2, los siguientes 12 a 18 meses serán fundamentales para validar su promesa comercial.
Fuente:
[1] IDEAYA Biosciences anuncia datos positivos de un ensayo combinado de fase 1/2 del medicamento IDE397 y el medicamento Trodelvy en cáncer urotelial con eliminación de MTAP.[https://www.prnewswire.com/news-releases/ideaya-biosciences-announces-positive-data-of-phase-12-combined-trial-of-ide397-a-potencial-first-in-class-mat2a-inhibitor-and-trodelvio-in-mtat-deletion-urothelial-cancer-302548584.html]
[2] Una revisión sistemática de la literatura acerca de las deleciones de MTAP en cánceres sólidos[https://www.sciencedirect.com/science/article/pii/S2468294225001029]
[3] Enfoques letales sintéticos para tumores eliminados por MTAP[https://pmc.ncbi.nlm.nih.gov/articles/PMC11664235/]
[4] IDEAYA Biosciences anuncia el primer paciente en el ensayo combinado de fase 1/2 de IDE397 en MTAP-Deletion NSCLC[[https://www.nasdaq.com/press-release/ideaya-biosciences-announces-first-patient-phase-1-2-combinación-ide-397-a-potencial-primero-en-clase-mat2a-inhibidor-y-trodelvio-en-mtap-deleción-no-cáncer-de-pulmón-de-células-pequeñas-302545937.html]
¿Cuándo recibirá la atención?5] IDEAYA Biosciences anuncia la presentación de un IND para el IDE892[[https://www.nasdaq.com/press-release/ideaya-biosciences-announces-ind-submission-ide892-potential-best-class-prmt5]
[6] IDEAYA Biosciences - Relaciones con inversores[ir.ideayabioIDYA--.com/]
[7] Las designaciones de terapias innovadoras aumentan a medida que las asociaciones de medicamentos para el cáncer de $50 mil millones remodelan el mercado[[https://www.prnewswire.com/news-releases/breakthrough-therapy-designs-surge-as-50b-cancer-drug-partnerships-reshape-market 302549075.html]
[8] Boston Biotech podría tener un informe de investigación de ventas de gran éxito[[https://www.streetwisereports.com/article/2024/01/03/boston-biotech-could-have-blockbuster-sales.html]
[9] Sacituzumab govitecan-hziy - Objetivos farmacológicos, indicaciones[[https://synapse.patsnap.com/drug/9ae626b75273433f8f4203ee3f7aa181]
[10] Tango Therapeutics: la interpretación de datos de PRMT5 que finaliza en 2025 es crítica[[crítico] http://seekingalpha.com/article/4792994-tango-therapeutics-fecha-llegada-a-lectura-de-datos-prmt5-en-2025
[11] El conjunto IDE397-Trodelvy de IDEAYA muestra una respuesta del 57 % en el cáncer urotelial con eliminación de MTAP[https://www.stocktitan.net/news/IDYA/ideaya-biosciences-announces-positive-data-from-phase-1-2-wwd6pylhwyz3.html]
[12] Impacto de la pérdida de MTAP en los resultados de la inmunoterapia en el mesotelioma pleural difuso[https://ascopubs.org/doi/10.1200/JCO.2025.43.16_adj.8081]

Comentarios
Aún no hay comentarios