Dyne Therapeutics: ¿Es la plataforma FORCE una infraestructura adecuada para el tratamiento de enfermedades neuromusculares?
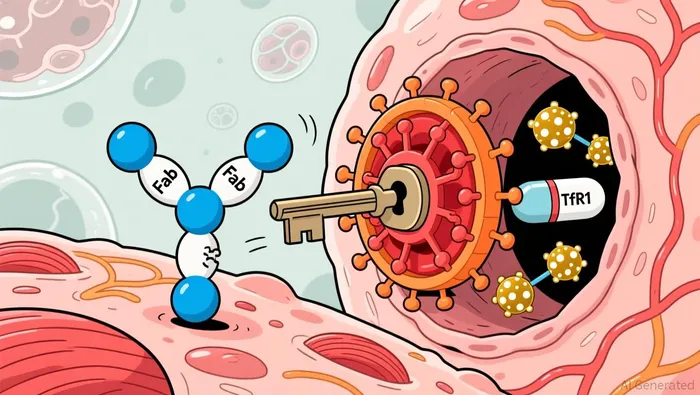
Dyne Therapeutics está construyendo una base tecnológica para el próximo paradigma en el tratamiento de las enfermedades neuromusculares. En su núcleo se encuentra la plataforma FORCETM, un sistema de administración dirigida, diseñado con un enfoque basado en los principios básicos, con el objetivo de superar un obstáculo fundamental: llevar las terapias hasta los lugares donde son más necesarias, es decir, hasta los músculos y el sistema nervioso central. La plataforma utiliza un pequeño fragmento de antígeno que se une al receptor de transferrina 1 (TfR1), presente en la superficie celular. Este fragmento actúa como una “llave molecular”, permitiendo el acceso de las sustancias terapéuticas a esos tejidos de difícil acceso.
El diseño es modular y está creado para un propósito específico. La plataforma está conectada a diversos tipos de cargas útiles, como oligonucleótidos antisententes, siRNA o incluso enzimas. Cada uno de estos componentes está diseñado para abordar directamente la causa genética de una enfermedad específica. Esta flexibilidad es clave. Al utilizar una plataforma como Fab en lugar de un anticuerpo completo, Dyne busca reducir la carga proteica, mejorar la penetración en los tejidos y, potencialmente, aumentar la tolerabilidad del producto. El potencial de esta plataforma se evidencia por el reconocimiento regulatorio que ha recibido; ha obtenido designaciones de “Breakthrough Therapy” tanto para su programa principal, z-rostudirsen, para la distrofia muscular de Duchenne, como para z-basivarsen, para la distrofia miotónica de tipo 1.
No se trata simplemente de una sola droga; se trata de una infraestructura potencial. Se estima que la población total de pacientes en los tres programas clínicos de Dyne –DMD, DM1 y enfermedad de Pompe– sea de más de 30,000 personas en Estados Unidos. Esta cantidad significativa de pacientes constituye un mercado muy importante para una plataforma que podría adaptarse a múltiples objetivos genéticos. La visión es que FORCE se convierta en el método estándar para la administración de terapias neuromusculares de próxima generación, al igual que un sistema ferroviario básico permite la implementación de un nuevo paradigma de transporte.
En resumen, las promesas de esta plataforma son enormes, pero su éxito depende de un factor crucial: demostrar una eficacia superior en los ensayos clínicos. Las designaciones de “Terapia Revolucionaria” son una muestra de confianza en los datos obtenidos inicialmente, pero no constituyen una garantía. El valor de esta plataforma solo se demostrará cuando logre mejorar significativamente la calidad de vida de los pacientes. De ese modo, se confirmará su posición como una verdadera infraestructura para el futuro de la medicina genética.
Progreso clínico y vías de regulación: Cómo navegar la curva de adopción
Dyne se encuentra ahora en un punto de inflexión crítico. La trayectoria clínica y regulatoria de la compañía determinará la velocidad con la que su plataforma será adoptada por los pacientes. La empresa ha establecido un plan claro para sus dos programas principales, cada uno de los cuales avanza hacia una posible solicitud de aprobación acelerada en los Estados Unidos. En cuanto a la distrofia muscular de Duchenne, se espera que los datos preliminares del grupo de estudio del ensayo DELIVER sean disponibles en diciembre de 2025. Estos datos serán el catalizador inmediato para una posible solicitud de licencia de uso de productos biológicos, con lo que se podría acelerar el proceso de aprobación a principios de 2026. La designación de “Terapia Revolucionaria” para z-rostudirsen (DYNE-251) proporciona un tránsito rápido en términos regulatorios, con beneficios como la revisión gradual y la elegibilidad para una revisión prioritaria, lo que podría reducir el tiempo necesario para obtener la aprobación.
En el caso de la distrofia miotónica tipo 1, el camino hacia la obtención de los resultados está un poco más largo, pero es igualmente claro. La inscripción en el grupo de pacientes para el estudio ACHIEVE está programada para completarse a principios del segundo trimestre de 2026. Este cambio en las directrices anteriores refleja una expansión estratégica de los centros de investigación, iniciada en septiembre. Lo más importante es que la empresa ha logrado obtener un importante apoyo regulatorio: la FDA ha aceptado un protocolo revisado, en el cual el tiempo necesario para abrir las manos con video se considera como el punto final principal para la aprobación acelerada en Estados Unidos. Esto representa una respuesta directa a la necesidad de tener un punto final clínico cuantificable y preciso, lo cual es un paso crucial hacia un proceso de aprobación más rápido.
Desde el punto de vista financiero, Dyne está en una posición favorable para enfrentar esta situación. La empresa ha reafirmado que su reserva de efectivo continúa hasta el tercer trimestre de 2027. Este respaldo es esencial, ya que le permite superar el período posterior al primer lanzamiento comercial de z-rostudirsen en el mercado DMD, lo cual la gerencia espera que ocurra a principios de 2027. Además, este respaldo también cubre la posibilidad de presentar una solicitud de autorización para el lanzamiento de z-basivarsen en el mercado DM1, algo que se espera que ocurra a finales de 2026.
La situación actual es clásica para una plataforma que está en la curva de adopción. El éxito en los próximos puntos de datos, como en diciembre de 2025 para DMD y a principios de 2026 para DM1, podría acelerar la entrada en el mercado y validar las expectativas de la plataforma FORCE. Si fracasa, o incluso si los resultados son insatisfactorios, eso probablemente ralentizará todo el proceso. La fortaleza financiera de la empresa ofrece un margen de seguridad, pero el rumbo del precio de las acciones estará determinado por los acontecimientos futuros. Los próximos dos trimestres mostrarán si Dyne puede pasar de un concepto prometedor a una realidad comercial.
Paisaje competitivo y riesgos relacionados con la adopción del mercado
El camino hacia una adopción exponencial de la plataforma FORCE de Dyne no es una línea recta. Es necesario navegar por un entorno competitivo en el que un único jugador dominante ya controla el mercado. Sarepta Therapeutics tiene una posición de liderazgo en este sector.Un 55-60% de las ventas en el mercado mundial de terapias para la enfermedad de Dejerine.Esta posición se ha consolidado gracias al tratamiento genético ELEVIDYS. Esto crea una barrera formidable para Dyne’s z-rostudirsen, si logra obtener la aprobación del mercado. El principal riesgo no es solo demostrar que el tratamiento tiene un significado estadístico, sino también probar que ofrece mejoras funcionales clínicamente significativas y duraderas. Esto justifica el pago de un precio más alto por el tratamiento, y además permite a Dyne’s z-rostudirsen ganar cuota de mercado frente a un líder con un producto exitoso.
Los datos clínicos recientes de la empresa ofrecen una ventaja potencial. En la próxima conferencia MDA, Dyne presentará sus resultados.Nuevas analizas indican una posible preservación de la función cardiopulmonar.A partir de su prueba en el estudio DELIVER, se han obtenido resultados sin precedentes en términos de mejoras funcionales. Este enfoque en los beneficios para múltiples sistemas podría ser un punto clave para la diferenciación de esta plataforma. Sin embargo, el éxito de la plataforma depende de cómo se traduzca este potencial en realidades comerciales. El mercado requerirá algo más que simplemente un nuevo mecanismo; se necesitará una clara ventaja en términos de eficacia, seguridad y conveniencia de uso.
Más allá de la batalla inmediata contra la distrofia muscular DMD, los programas preclínicos de Dyne relacionados con la distrofia muscular facioscapulohumeral (FSHD) y la enfermedad de Pompe representan un potencial de crecimiento a largo plazo. Estos programas amplían el alcance de la plataforma hacia nuevos objetivos genéticos, lo que refuerza su capacidad de desarrollo. Sin embargo, también implican mayores incertidumbres técnicas y regulatorias. El trabajo preclínico está lejos de alcanzar la validación clínica, y cada nueva enfermedad aumenta la complejidad del cronograma de desarrollo y las necesidades de capital.
En resumen, las amenazas competitivas y los riesgos relacionados con la adopción de la tecnología son los principales obstáculos que dificultan el desarrollo de la curva exponencial de Dyne. La empresa debe no solo ganar las pruebas clínicas, sino también ganar el mercado. Su capacidad para demostrar resultados funcionales superiores y duraderos será determinante para determinar si la plataforma FORCE se convertirá en el nuevo estándar o seguirá siendo una alternativa prometedora en un campo tan competitivo como este.
Catalizadores, escenarios y lo que hay que observar
La próxima fase para Dyne está definida por una serie de objetivos claros y a corto plazo, que servirán para validar o poner a prueba toda la plataforma desarrollada por la empresa. El éxito depende de la transformación de los datos preliminares prometedores en indicadores regulatorios y clínicos concretos. El factor clave para el éxito es…Datos totales obtenidos de la cohorte de expansión registral del estudio DELIVER.Se espera que esta información se haya disponible en diciembre de 2025. Este dato determinará la solidez del argumento presentado por el programa DMD para obtener la aprobación acelerada por parte de los Estados Unidos. La trayectoria de las acciones estará directamente relacionada con si estos datos demuestran no solo un significado estadístico, sino también una mejora funcional sin precedentes, lo cual podría justificar un precio más alto que el de los competidores.
El siguiente punto de control es…Marzo de 2026: Conferencia Clínica y Científica MDAEste evento constituye una señal importante para el futuro de la plataforma. Dyne presentará nuevos análisis obtenidos del estudio DELIVER, incluyendo información sobre la posibilidad de preservar la función cardíaca y pulmonar. Este beneficio multisistémico es un aspecto clave que diferencia a la plataforma de otras alternativas. Al mismo tiempo, la empresa presentará el diseño de un ensayo de fase 3 para el uso de z-basivarsen en pacientes con DM1. La calidad y ambición de este ensayo revelarán la confianza que Dyne tiene en el potencial de la plataforma para este segundo indicador clínico importante.
En el programa DM1, el enfoque se centra en la retroalimentación regulatoria. La empresa ya ha dado un paso importante hacia este objetivo.Se propone un protocolo revisado en el cual el tiempo de apertura de la mano durante la grabación de video (vHOT) se considera como el objetivo principal.Para obtener la aprobación acelerada por parte de los Estados Unidos, lo siguiente que hay que esperar es la respuesta del FDA. Cualquier tipo de retroalimentación positiva o aceptación de este punto final sería una importante aceleración en el proceso de lanzamiento al mercado, lo cual validaría la estrategia de la empresa. La finalización de la participación en el grupo de expansión del estudio ACHIEVE, a principios del segundo trimestre de 2026, también constituye un hito operativo importante que debe ser monitoreado.
En resumen, estas son las métricas que se utilizan para monitorear la adopción de la plataforma. Cada hito en el camino hacia la adopción representa un punto clave en la curva de adopción. Los datos de diciembre de 2025 son una prueba crucial. Los datos obtenidos durante la conferencia de marzo sirven como validación inicial de la eficacia de la plataforma. La alineación con los requisitos regulatorios relacionados con el endpoint DM1 vHOT es el paso final para lograr una adopción rápida de la plataforma. Si se logra éxito en estos puntos, Dyne podrá pasar de ser una empresa en etapa clínica a convertirse en una plataforma con una trayectoria comercial clara. Si se falla o hay vacilaciones en algún paso del proceso, eso probablemente retarde todo el proceso de adopción de la plataforma.



Comentarios
Aún no hay comentarios