El stack IO+ADC 2.0 de Akeso entra en la fase II de su desarrollo: los productos de la línea Combo son los primeros en someterse a pruebas clínicas importantes.
Olvídense de las actualizaciones incrementales. Akeso acaba de superar su primer gran obstáculo clínico en su plataforma, una tecnología que podría convertirse en algo realmente revolucionario… o, por el contrario, ser solo una distracción costosa. La señal es clara: la empresa está lanzando su tecnología “IO 2.0 + ADC 2.0” en la fase II de su desarrollo. No se trata simplemente de otro ensayo clínico; se trata de una validación de alto riesgo para una solución única y completa.
Aquí está el informe de filtración del prototipo: Akeso es la única empresa global que cuenta con dos anticuerpos bispecíficos aprobados para su uso en terapias médicas (cadonilimab y ivonescimab). Se trata de una combinación muy rara. Actualmente, esta empresa utiliza esos anticuerpos como base para crear nuevos ADCs, como AK146D1 y AK138D1. La fase II de los ensayos clínicos de ambos ADCs representa la primera validación importante de toda esta plataforma tecnológica. Si estas combinaciones funcionan, se tratará de una gran ventaja competitiva. Pero si no funciona, será un desafío costoso. Estén atentos a las primeras pruebas en el mundo real.
El desglose: Señal contra ruido
Vamos a dejar de lado ese lenguaje técnico empresarial. La aprobación en la Fase II es algo real, pero ¿qué se está probando exactamente? ¿Y por qué es importante eso? Esta es la realidad clínica y comercial que está detrás del éxito de esta plataforma.
En primer lugar, los propios activos. La señal que emite estos activos se debe a su novedad y a su capacidad de dirigirse hacia objetivos específicos.
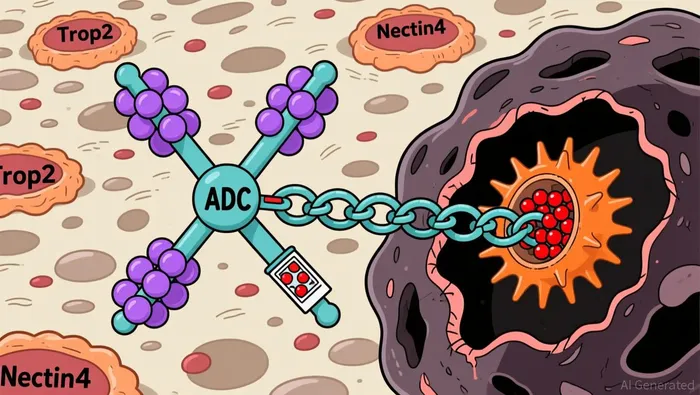
- AK146D1 es un ADC bispecífico de tipo Trop2/Nectin4 de primer nivel. Es decir, se trata del primer medicamento que logra alcanzar ambos objetivos simultáneamente. Ambos antígenos se encuentran altamente expresados en los tumores sólidos comunes, como los cánceres de pulmón, mama y vejiga. Sin embargo, su expresión es baja en los tejidos sanos, lo cual es ideal para una terapia dirigida. El diseño de doble objetivo permite ampliar el rango terapéutico y superar las resistencias observadas en los ADC con un solo objetivo. Se trata de una iniciativa pura y sin compromisos, en un campo prometedor.
 AK138D1 es un ADC dirigido a la proteína HER3. HER3 representa una necesidad médica que aún no ha sido satisfecha. Aunque los medicamentos experimentales han tenido dificultades durante décadas, las investigaciones recientes destacan el papel importante que juega esta proteína en el desarrollo del cáncer. El enfoque de Akeso consiste en utilizar su experiencia en el desarrollo de ADCs para lograr alcanzar este objetivo. Esto podría ser un factor importante a favor de Akeso si tiene éxito.
AK138D1 es un ADC dirigido a la proteína HER3. HER3 representa una necesidad médica que aún no ha sido satisfecha. Aunque los medicamentos experimentales han tenido dificultades durante décadas, las investigaciones recientes destacan el papel importante que juega esta proteína en el desarrollo del cáncer. El enfoque de Akeso consiste en utilizar su experiencia en el desarrollo de ADCs para lograr alcanzar este objetivo. Esto podría ser un factor importante a favor de Akeso si tiene éxito.
En segundo lugar, está la estrategia de combinación. Es aquí donde el “stack” propio de cada jugador se vuelve realmente importante.
Los ensayos de fase II no evalúan estas ADCs de forma independiente. Estas ADCs se están evaluando en combinación con los activos IO 2.0 de Akeso: cadonilimab e ivonescimab. Esto crea un conjunto terapéutico completamente desarrollado internamente por la empresa. La compañía apuesta por la combinación de sus dos anticuerpos bispecíficos aprobados con sus nuevas ADCs, lo que podría generar efectos sinérgicos y superar las limitaciones de la monoterapia, como la capacidad de los antígenos para evadir el sistema inmunitario y la heterogeneidad de los tumores.
En resumen: se trata de una validación de gran importancia para una tecnología única. Akeso es la única empresa mundial que cuenta con dos anticuerpos bispecíficos aprobados. Ahora, utiliza esa combinación única para impulsar su pipeline de productos ADC. El lanzamiento en Fase II tanto de AK146D1 como de AK138D1 representa el primer ensayo clínico importante de toda esta plataforma patentada. Si estas combinaciones funcionan, se tratará de una ventaja competitiva importante. Pero si no funciona, significará un giro costoso en su estrategia de negocios. La situación es clara: la empresa está pasando su plataforma de la etapa conceptual a la etapa clínica.
La lista de vigilancia: Factores catalíticos y riesgos
La plataforma está en funcionamiento. Ahora, el mercado juzgará su rendimiento clínico. Estos son los aspectos que hay que tener en cuenta durante los próximos 18-24 meses.
El principal catalizador: los resultados de los datos obtenidos en la Fase II El acontecimiento más importante que se avecina es la recepción de los primeros datos clínicos obtenidos de estos ensayos de Fase II. La empresa acaba de recibir la autorización para lanzar el producto al mercado.Ensayos clínicos de fase II para AK146D1 y AK138D1Los resultados de estas combinaciones, que se esperan en los próximos 18-24 meses, serán la prueba definitiva de la eficacia del sistema IO+ADC 2.0. Si los datos son positivos y demuestran una efectividad clara, además de un perfil de seguridad manejable, entonces toda la estrategia de la plataforma será validada. Esto, a su vez, podría llevar a un aumento en el precio de las acciones de la empresa. Se trata de una situación en la que la información “alfa” se convierte en una prueba concreta de la eficacia del sistema.
El mayor riesgo es el fracaso clínico. Por otro lado, existe también el riesgo de que estas combinaciones no ofrezcan beneficios claros. Tanto el AK146D1 como el AK138D1 son productos de primera generación o de nueva tecnología. Si los datos de la fase II solo muestran mejoras marginales en comparación con los tratamientos existentes, o si se descubren problemas significativos relacionados con la seguridad del producto, esto podría reducir la valía de toda esta estrategia. La estrategia depende de la sinergia entre los componentes utilizados; si esa combinación no funciona, el producto perderá su ventaja competitiva. Este es el verdadero problema en este caso.
Procure seguir los avances en las regulaciones. Además de los datos clínicos, es importante mantenerse al tanto de los avances regulatorios en los mercados clave. La empresa ya ha obtenido aprobaciones en China, Estados Unidos y Australia para iniciar los ensayos clínicos. El siguiente paso es que estos ADCs nuevos obtengan la aprobación regulatoria como terapias combinadas. La aprobación global es crucial para su comercialización. Cualquier progreso en Estados Unidos u otros mercados importantes será un factor positivo; por otro lado, cualquier retraso podría dificultar el proceso de comercialización.
En resumen: La lista de objetivos es sencilla: los datos de la Fase II, en un plazo de 18 a 24 meses, son el factor decisivo que podría marcar el éxito o el fracaso de la plataforma. El riesgo de fracaso clínico es real y podría arruinar todo el proyecto. Mientras tanto, los avances regulatorios en el extranjero son una señal importante, aunque secundaria. Aquí es donde convergen los logros técnicos con los resultados clínicos.
En resumen: Qué ver.
El lanzamiento en la Fase II representa un evento binario. El éxito valida una plataforma única; el fracaso, por otro lado, podría reajustar la valoración de la misma. Este es tu lista de observación, con información útil para tomar decisiones.
La apuesta binaria: validación de la plataforma o pivote Se trata de una prueba decisiva. Akeso es la única empresa mundial que cuenta con dos anticuerpos bispecíficos aprobados para su uso en terapias farmacológicas. Ahora, Akeso está apostando toda su estrategia IO+ADC 2.0 en dos nuevos anticuerpos bispecíficos, AK146D1 y AK138D1, en combinación con esos anticuerpos. La fase II de las pruebas representa el paso decisivo para demostrar la eficacia de esta combinación. Si los resultados son positivos, esto fortalecerá la posición competitiva de Akeso. Por otro lado, si los resultados son insatisfactorios o surgen problemas relacionados con la seguridad, eso podría debilitar la reputación de la plataforma y, probablemente, afectar negativamente al precio de sus acciones. Este es un indicador clave que hay que observar atentamente.
Datos de la Fase II: Busquen la sinergia, no solo la actividad. Los primeros resultados clínicos en un plazo de 18 a 24 meses serán el indicador principal. No busquen simplemente cualquier tipo de eficacia. Estén atentos a señales de sinergia entre los diferentes componentes del tratamiento.
- Tasas de respuesta mejoradas: ¿Los regímenes combinados presentan tasas de respuesta más altas en comparación con los datos históricos correspondientes a agentes utilizados por separado o al estándar de tratamiento habitual?
- Seguridad manejable: ¿El perfil de seguridad es adecuado? El diseño de doble objetivo tiene como objetivo lograr un rango terapéutico más amplio. ¿Los datos respaldan esto?
Superando la resistencia: ¿Son las pruebas que muestran actividad en los tumores los indicios de que estos podrían ser resistentes a las terapias dirigidas a un único objetivo? Este es el beneficio prometido de tratar con Trop2/Nectin4 o HER3.
Marcos regulatorios globales: El motor de la comercialización Los datos clínicos son la base científica. El progreso en las cuestiones regulatorias es el verdadero motor de la comercialización. La empresa ya ha obtenido autorizaciones para iniciar pruebas en los Estados Unidos, Australia y China. El siguiente paso crucial es que estos nuevos ADCs, especialmente cuando se utilizan como terapias combinadas, logren obtener aprobación regulatoria en los mercados clave. Cualquier decisión positiva en materia regulatoria, ya sea en los Estados Unidos o en otros mercados importantes, será un gran impulso para la comercialización. Por el contrario, cualquier retraso o obstáculo en los trámites regulatorios podría debilitar las perspectivas de comercialización de esta estrategia.
En resumen: La lista de vigilancia es clara. Los datos de la fase II, que se espera que estén disponibles en los próximos 18-24 meses, serán el punto de prueba definitivo. Es necesario monitorear cualquier señal de sinergia entre los productos. También es importante seguir los avances regulatorios mundiales relacionados con cadonilimab e ivonescimab, ya que estos son factores clave para la comercialización de esta estrategia combinada. Aquí es donde la plataforma realiza su primer verdadero test en el mundo real.



Comentarios
Aún no hay comentarios